Ben je geïnteresseerd in de wereld van wetenschap & technologie en wil je hier graag meer over lezen? Word dan lid van KIJK!
Deze maand is het tien jaar geleden dat de genbewerkingsmethode CRISPR-Cas9 werd geïntroduceerd. Maar wie ontwikkelde de techniek en hoe werkt het überhaupt? KIJK praat je bij.

De biomedische wereld kende de afgelopen decennia heel wat mijlpalen. Een van de spannendste ontwikkelingen voltrok zich rond DNA. Het startschot kwam van de Amerikaan Marshall Nirenberg (foto rechts): die had net de code van het DNA-molecuul gekraakt en ontving in 1968 daarvoor de Nobelprijs voor de geneeskunde.
Wanneer werd DNA voor het eerst bewerkt?
Toen DNA, de software van het leven, kon worden afgelezen en misschien zelfs herschreven, brak een nieuw tijdperk aan voor de biologie én de medische wereld. De eerste DNA-bewerking liet niet lang op zich wachten. In 1973 plakten Stanford-wetenschappers bewerkt DNA voor het eerst in een levend wezen, een E. coli-bacterie. Dat bleek zo schrikbarend eenvoudig dat wetenschappers wereldwijd afspraken niet zomaar met het leven te knoeien.
Terwijl het daardoor in de rest van de jaren zeventig op het DNA-front relatief stil bleef, boekte de medische wereld vooruitgang. De eerste reageerbuisbaby kwam in 1978 ter wereld. En door slimmere labtechnieken en kennis van ons afweersysteem begon de mensheid gericht ziekteverwekkers aan te pakken. Een doorbraak die miljoenen mensen zou redden, was de ontdekking van hiv in 1983. Later werden met DNA-technieken de eerste hiv-medicijnen ontwikkeld.
Halverwege de jaren tachtig raakte de DNA-wereld alsnog in een stroomversnelling. Dankzij een nieuwe techniek die PCR heet, valt de genetische code vliegensvlug af te lezen. Bewerken werd ook steeds preciezer, en zelfs mogelijk in complexe organismen zoals planten en dieren. Genetisch gemodificeerde gewassen begonnen de landbouw te veroveren. Voor het eerst werden foetussen getest op erfelijke ziektes. Maar terwijl wetenschappers langzamerhand grip op de DNA-code kregen, moest de grootste klapper nog komen.
Wie ontdekten CRISPR-Cas?
In 2012 was het zover: toen stuitten Jennifer Doudna en Emmanuelle Charpentier op een bijzonder DNA-schaartje, genaamd Cas9. Ze realiseerden zich dat die valt ‘op te hangen’ aan het vernuftige bacterieafweersysteem CRISPR, dat een soort TomTom-achtige trucje kent voor het navigeren naar bepaalde DNA-codes. De combinatie werkte verbluffend: een onderzoeker hoeft sindsdien alleen maar aan te wijzen welk stukje DNA hij of zij wil herschrijven, en CRISPR-Cas9 doet de rest. Wat ooit jaren kostte, kan nu binnen een week.
Aan genen sleutelen gaat tegenwoordig zo rap en makkelijk dat het biomedische uitvindingen en sterkere landbouwgewassen regent. De eenvoud ervan schrikt onderzoekers opnieuw af. Ditmaal roepen ze op om een grens te trekken bij het kweken van DNA-bewerkte supermensen, met bijvoorbeeld sterkere spieren of botten. Of iedereen zich daaraan houdt, is een tweede: het boek des levens laat zich nu wel érg gemakkelijk herschrijven.

Hoe werkt CRISPR-Cas?
Sleutelen aan het DNA gebeurt dus al jaren. Maar in tegenstelling tot de andere technieken – die het tempo hebben van paard en wagen – maakt CRISPR-Cas DNA-bewerkingen met straaljagersnelheid mogelijk. Vóór het CRISPR-tijdperk – dat wil zeggen: tot 2013 – had je als onderzoeker zo’n vijf jaar nodig om tientallen genen in een cel te bouwen. Met CRISPR kan het in twee weken. En het trucje werkt ook nog eens bij alle microben, planten en dieren, inclusief mensen.
CRISPR-Cas werkt zo snel en efficiënt doordat de techniek het meeste werk door de cel zelf laat doen. Het Cas-gedeelte is een moleculair schaartje dat het DNA op een precieze plek openknipt; de cel gaat het vervolgens meteen repareren. Het gat vult hij daarna op met een DNA-code uit de CRISPR-module, die dan toch al voorhanden is. Klaar is Kees.
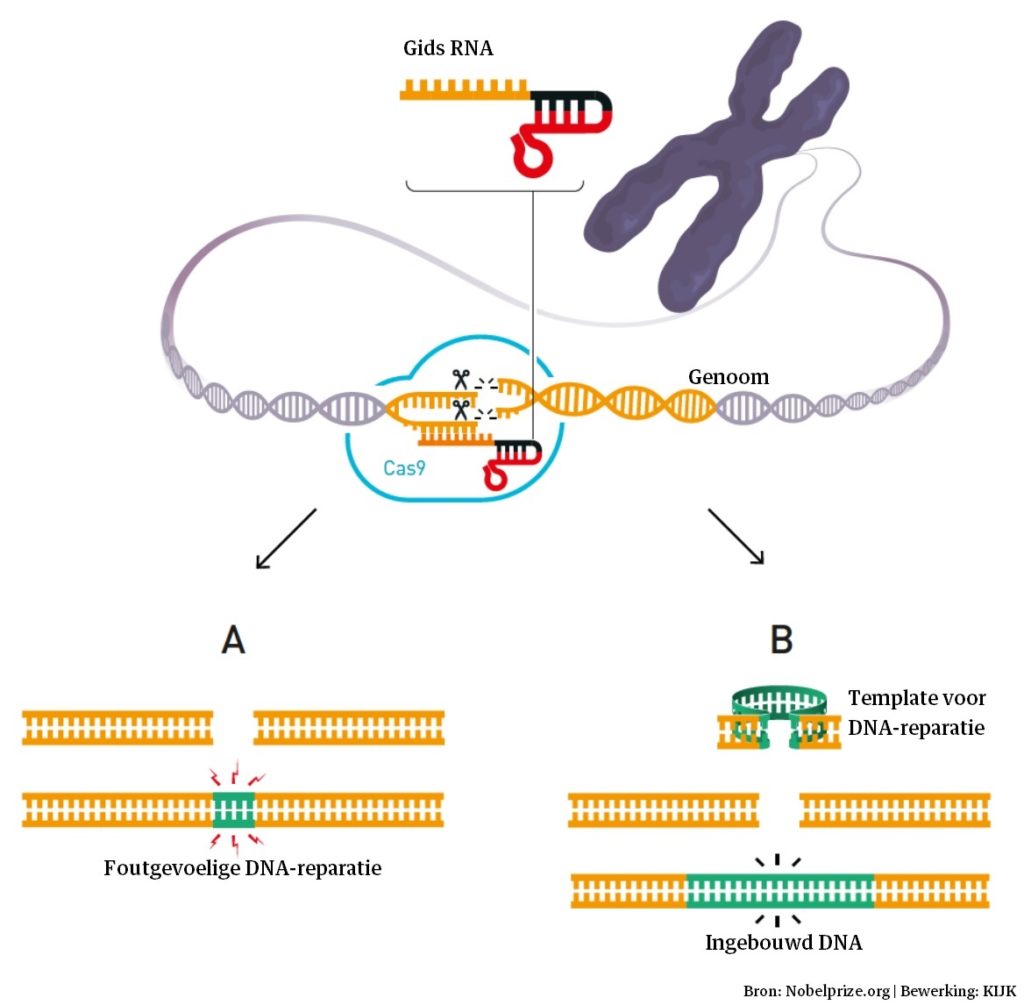
Op deze manier helpt de techniek onderzoekers razendsnel om DNA-reparaties uit te voeren en medische vragen te beantwoorden. Sinds Charpentier en Doudna deze knip-en-plak-techniek in 2012 ontwikkelden, hebben veel vakgebieden er al gebruik van gemaakt. Zo was hoogleraar stamcelbiologie in Utrecht, Hans Clevers, een van de eersten die CRISPR gebruikte: zijn team genas er opgekweekte darmen mee van taaislijmziekte.
Ook andere vragen over hoe ons genoom werkt om bijvoorbeeld kanker te bestrijden, krijgen dankzij de nieuwe techniek een enorme boost. Een paar genen in- of uitschakelen om te zien hoe een tumor reageert, is nu zo gepiept. Bovendien zijn plantenonderzoekers erin geslaagd om met behulp van CRISPR gewassen te ontwikkelen die bestand zijn tegen plagen en droogte.
In 2020 ontvingen Charpentier en Doudna de Nobelprijs voor de scheikunde voor deze hogere knip- en plakkunde.
Bronnen: KIJK 8/2018, KIJK Zomernummer 2020, Nobelprize.org
Beeld: Natali Mis/iStock/Getty Images